Anvisa autoriza estudos clínicos sobre 3° dose da vacina AstraZeneca e uso da proxalutamida para tratamento da Covid-19
O presidente Bolsonaro defende o uso do medicamento
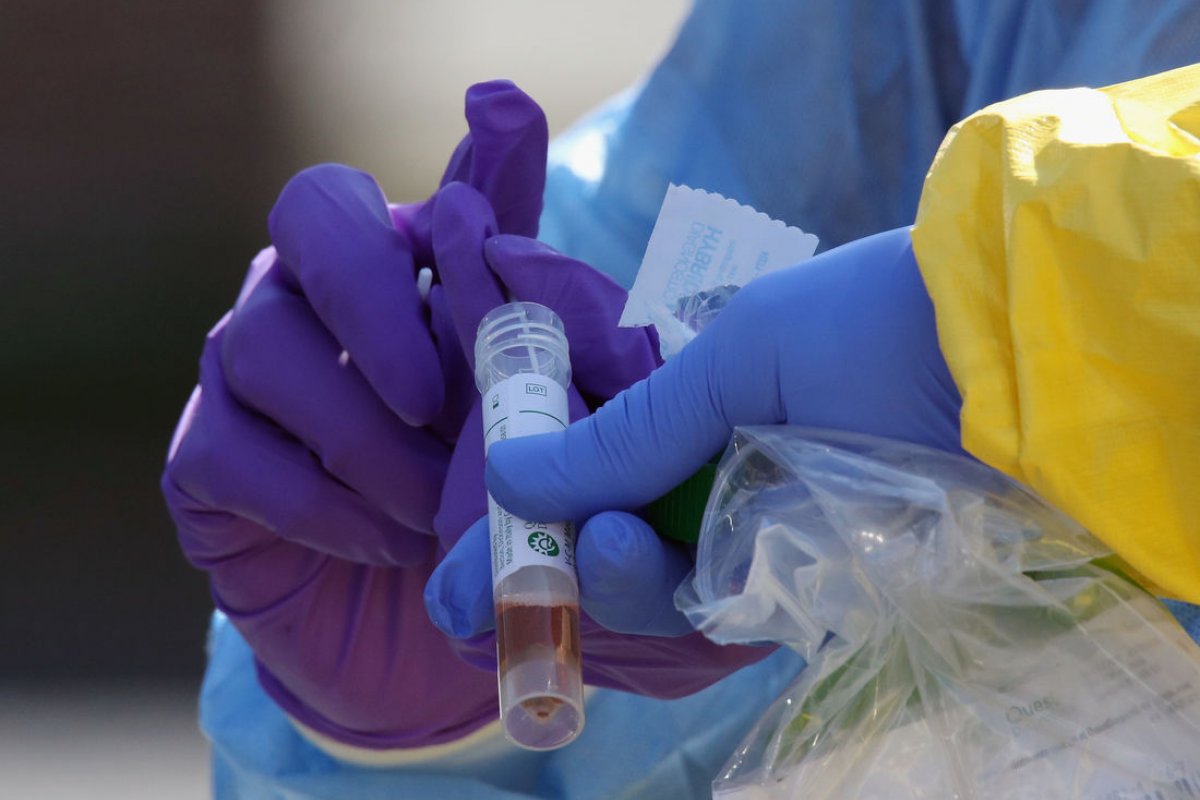
Foto: Getty Images
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou, nesta segunda-feira (19), a realização de um estudo clínico para avaliar a segurança, a eficácia e a imunogenicidade de uma terceira dose da vacina da AstraZeneca contra a Covid-19, doença causada pelo novo coronavírus. Além disso, a agência reguladora também aprovou a realização de um estudo clínico para avaliar a segurança e a eficácia do medicamento proxalutamida na redução da infecção viral causada pelo vírus. No último domingo (18), o presidente Jair Bolsonaro (sem partido) defendeu o medicamento como eficaz para o tratamento da doença.
Trata-se de um estudo de fase III, randomizado, duplo-cego, controlado por placebo, para avaliar a eficácia e a segurança da substância em participantes ambulatoriais do sexo masculino com Covid-19. O estudo é patrocinado pela empresa Suzhou Kintor Pharmaceuticals, sediada na China, e será realizado na Alemanha, Argentina, África do Sul, Ucrânia, México, Estados Unidos e Brasil. No total, participarão do estudo 12 voluntários do estado de Roraima e outros 38 de São Paulo.
AstraZeneca
A terceira dose da vacina da AstraZeneca será aplicada entre 11 e 13 meses após a segunda dose. Trata-se de um estudo de fase III, controlado, randomizado, simples-cego, ou seja, em que só o voluntário não saberá o que tomou: se uma dose da vacina ou de placebo. Serão incluídos voluntários com idade entre 18 e 55 anos, que estejam altamente expostos à infecção com o novo coronavírus, como profissionais de saúde. Não serão incluídas gestantes ou pessoas com comorbidades. O estudo, patrocinado pela AstraZeneca, será realizado somente no Brasil, nos estados da Bahia (1.500 voluntários), Rio de Janeiro (1.500 voluntários), Rio Grande do Sul (3.000 voluntários), Rio Grande do Norte (1.500 voluntários) e São Paulo (2.500 voluntários).
Na semana passada, a Anvisa tinha autorizado um estudo clínico com a vacina AstraZeneca AZD2816, uma nova versão do produto atualmente disponível no Brasil (AZD1222), modificada para também fornecer imunidade contra a recém-emergente cepa da variante B.1.351 do Sars-CoV-2, identificada primeiro na África do Sul.


