Saiba quais foram as condições para Anvisa aprovar a Sputnik V e Covaxin
Só 1% de cada estado do nordeste poderá tomar a vacina russa
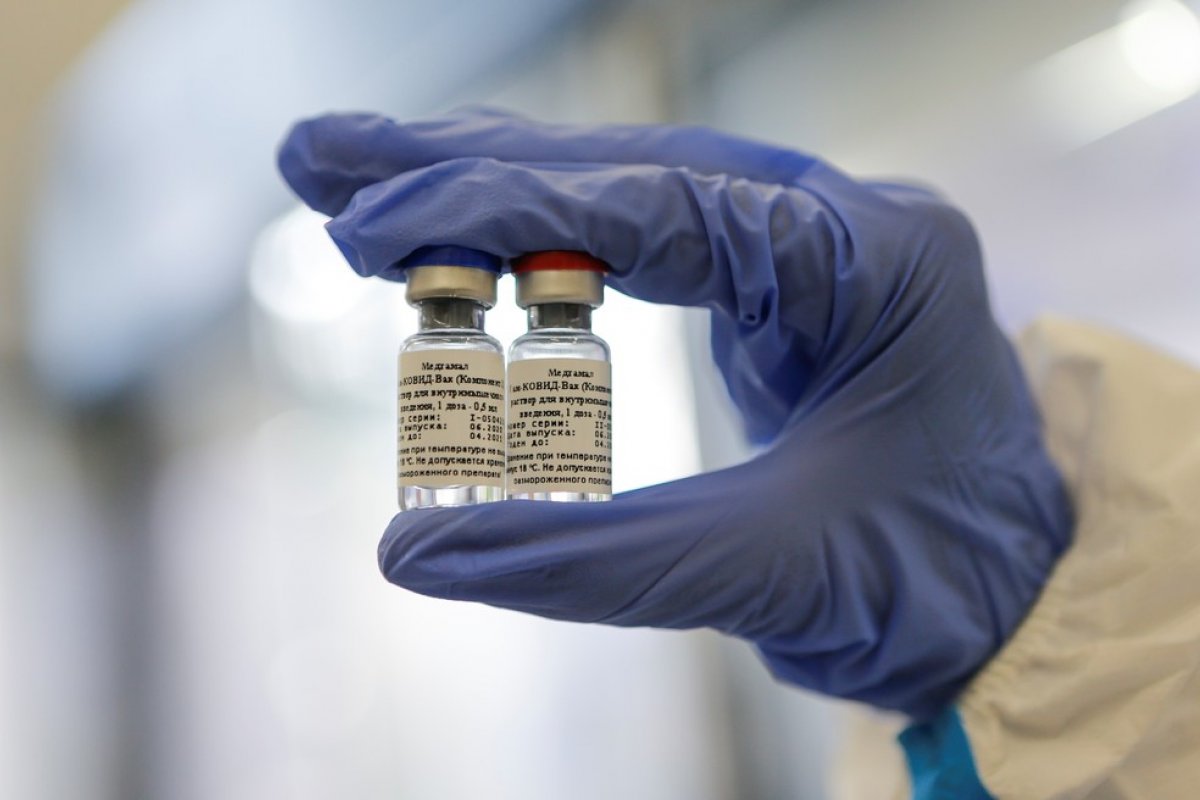
Foto: Reprodução/G1
A Agência Nacional de Vigilância Sanitária (Anvisa), aprovou o pedido de importação excepcional das vacinas Sputnik V e Covaxin contra a Covid-19 nesta sexta-feira (4).
A Sputnik V que foi desenvolvida na Rússia é uma vacina de vetor viral (mesma tecnologia de Oxford/AstraZeneca e Johnson), ela é aplicada em duas doses com diferença de até 3 meses entre elas. O imunizante possuí 91.6% de eficácia segundo estudo de fase 3.
A Covaxin, desenvolvida na Índia, tem a mesma tecnologia da CoronaVac, uma vacina inativada. Ela é aplicada em duas doses com diferença de 2 a 4 semanas. Dados preliminares de fase 3 apontam que a vacina possuí 78% de eficácia.
A Anvisa autorizou a importação excepcional dos lotes solicitados das vacinas, podendo ser importadas pelo Ministério da Saúde (no caso da Covaxin) ou pelos estados (no caso da Sputnik V) e aplicadas. A autorização é apenas para às doses importadas e aquelas fabricadas em plantas inspecionadas pela Anvisa.
A agência não autorizou o uso emergencial de nenhuma das duas vacinas.
A Sputnik V apresentou dados que mostram que sua vacina é segura e eficaz contra a Covid. Já a Covaxin não teve estudos de fase 3 publicados, mas um anúncio feito pela própria fabricante da vacina apontou que a vacina foi eficaz contra a Covid.
928 mil doses da Sputnik V foi autorizado pela Anvisa em 6 estados, sendo eles: Bahia, Maranhão, Sergipe, Ceará, Pernambuco, Piauí. Apenas 1% da população de cada estado poderá tomar a vacina russa.
A Covaxin recebeu autorização de importação para 4 milhões de doses, que serão entregues ao Ministério da Saúde.
A Anvisa barrou o uso das doses dos lotes importados da Covaxin e Sputnik V para :os seguintes casos:
- Pessoas com hipersensibilidade a qualquer dos componentes da fórmula
- Gravidez
- Lactantes
- Menores de 18 anos ou maiores de 60 anos
- Mulheres em idade fértil que desejam engravidar nos próximos 12 meses
- Enfermidades graves ou não controladas e antecedentes de anafilaxia
- Pessoas que tenham recebido outra vacina contra a Covid-19
- Pessoas com febre
- Pessoas com HIV, hepatite B ou C
- Pessoas que tenham se vacinado nas 4 semanas anteriores
- Pessoas que tenham recebido imunoglobulinas ou hemoderivados 3 meses antes
- Pessoas que tenham recebido tratamentos com imunossupressores, citotóxicos, quimioterapia ou radiação 36 meses, tenham recebido terapias com biológicos incluindo anticorpos anticitocinas e outros anticorpos.


